Cientistas transformaram água pura em metal!
Em uma nova pesquisa, químicos do Instituto de Química Orgânica e Bioquímica da Academia de Ciências Tcheca e de outros lugares descobriram que uma solução de água metálica pode ser preparada por dopagem massiva com elétrons ao reagir água com metais alcalinos.

A água pura é um isolante quase perfeito. Sim, a água encontrada na natureza conduz eletricidade por causa das impurezas nela, que se dissolvem em íons livres e permitem o fluxo de correntes elétricas. A água pura só se torna “metálica” — eletronicamente condutora — em pressões extremamente altas que vão além de nossa capacidade atual.
Porém, como os pesquisadores demonstraram pela primeira vez, não são apenas as altas pressões que podem induzir essa condição na água pura. Ao colocar a água pura em contato com um metal alcalino compartilhando elétrons — neste caso uma liga de sódio e potássio — partículas carregadas de movimento livre podem ser adicionadas, tornando a água metálica.
O professor Jungwirth e seus colegas da República Tcheca, Estados Unidos, Alemanha, Egito e Japão expuseram uma gota de liga de sódio-potássio (NaK) a uma pequena quantidade de vapor d'água, que começou a condensar em sua superfície.
A condutividade resultante dura apenas alguns segundos, mas é um passo significativo entender essa fase da água ao estudá-la diretamente.
Sob pressões altas o suficiente, praticamente qualquer material poderia, teoricamente, se tornar condutor. A ideia é que, se você espremer os átomos com força suficiente, as órbitas dos elétrons externos começarão a se sobrepor, permitindo que eles se movam. Para a água, essa pressão é de cerca de 48 megabares, cerca de 48 milhões de vezes a pressão atmosférica da Terra ao nível do mar.
Um grupo de cientistas de Química Orgânica e Bioquímica de vários países conseguiram transformar água pura em metal dentro de uma câmara a vácuo controlando as condições de pressão. pic.twitter.com/XPlxbJaJgk
— Davi Moura (@DaviMoura__) July 31, 2021
Embora pressões que excedam isso tenham sido geradas em um ambiente de laboratório, tais experimentos seriam inadequados para estudar água metálica. Assim, uma equipe de pesquisadores liderada pelo químico orgânico Pavel Jungwirth, da Academia de Ciências Tcheca, voltou-se para os metais alcalinos.
Essas substâncias liberam seus elétrons externos com muita facilidade, o que significa que podem induzir as propriedades de compartilhamento de elétrons da água pura altamente pressurizada sem as altas pressões. Há apenas um problema: os metais alcalinos são altamente reativos com água líquida, às vezes até o ponto de explosão.

A equipe de pesquisa encontrou uma maneira muito bacana de resolver esse problema. E se, em vez de adicionar o metal à água, fosse adicionada água ao metal? Em uma câmara a vácuo, a equipe começou realizando a extrusão em um bico de uma pequena bolha de liga de sódio-potássio, que é líquida à temperatura ambiente, e com muito cuidado adicionou uma fina película de água pura usando deposição de vapor.
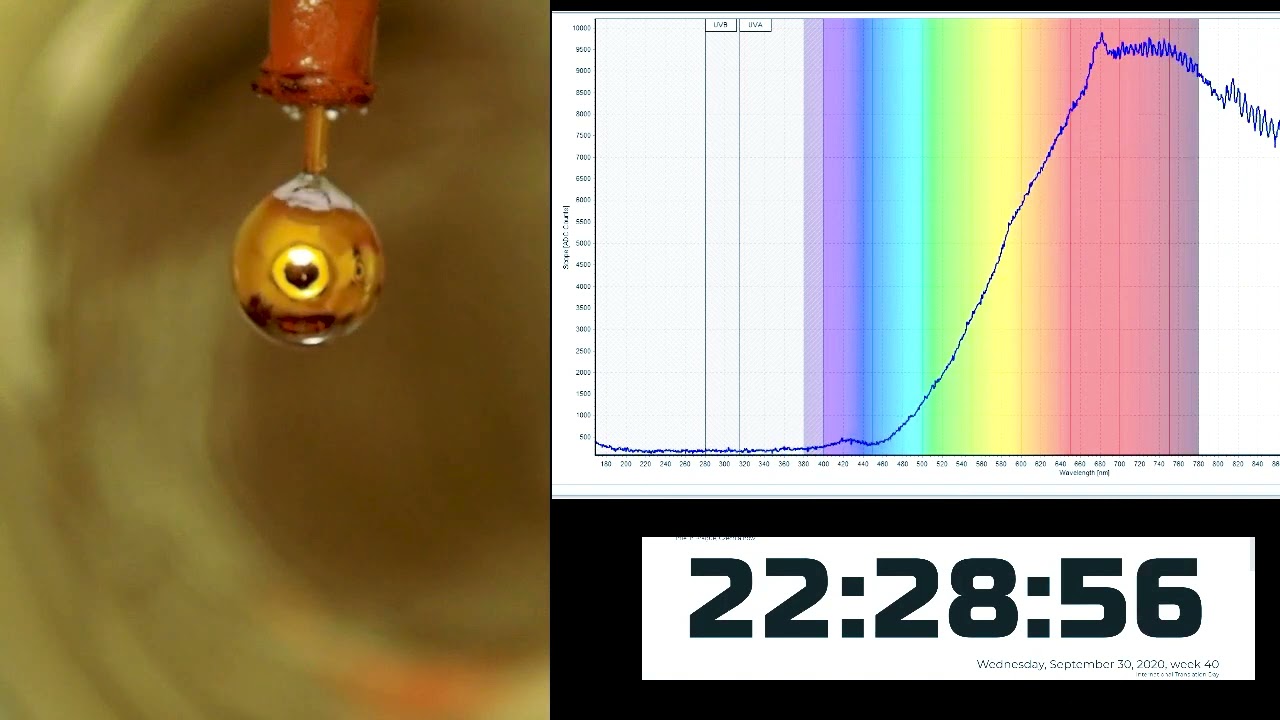
O contato entre a água e o metal faz que os elétrons e cátions metálicos (íons carregados positivamente) fluam da liga para a água. Isso não apenas fez a água ficar dourada, mas também deixou a água com condutividade; exatamente como deveríamos ver na água pura metálica em alta pressão.
Isso foi confirmado usando espectroscopia de reflexão óptica e espectroscopia de fotoelétrons de raios-X síncrotron. As duas propriedades — o brilho dourado e a banda condutiva — ocupavam duas faixas de frequência diferentes, o que permitia que ambas fossem identificadas com clareza.
Além de nos dar uma melhor compreensão dessa transição de fase aqui na Terra, a pesquisa também poderia permitir um estudo detalhado das condições de extrema alta pressão dentro de grandes planetas.




